
Historia de la química moderna
“El estudio de las partículas más pequeñas de la materia”
Durante mil años, los alquimistas buscaron la forma de transformar metales vulgares en oro. Lo intentaron aproximadamente desde el siglo VII hasta el XVII, primero en los países islámicos y después en Europa.

En el siglo XVII los alquimistas, ya desacreditados, cambiaron su nombre por el de químicos, y la alquimia pasó a llamarse química. Su abanderado fue el científico inglés Robert Boyle, autor de “El químico escéptico” publicado en 1661, donde ridiculizaba la idea aceptada de que todos los materiales estaban compuestos por los mismos cuatro elementos: tierra, aire, agua y fuego.
A comienzos del siglo XIX, el químico inglés John Dalton reanimó el concepto de «átomos», palabra acuñada en el siglo V a.C. por el filósofo griego Demócrito para designar las partículas de materia más pequeñas e indivisibles. Dalton sostenía que cada elemento estaba formado por un tipo particular de átomos, que podían combinarse para formar compuestos. La diferencia básica entre unos átomos y otros era el peso.
1813 el químico Johan Jakob Berzelius, propuso los símbolos atómicos, que aún seguimos usando, basados en la primera letra del nombre en latín, acompañada por una segunda letra cuando es necesario. Berzelius realizó, además, el primer intento sistemático de medir pesos atómicos. El concepto de átomos y moléculas -agrupaciones de dos o más átomos proporcionó a los químicos un instrumento de trabajo, pero su realidad física seguía mostrándose evasiva.
Durante todo el siglo XIX, la teoría de Dalton encontró mucha oposición, y el «atomismo» no triunfó hasta principios del siglo XX. Para entonces, el químico ruso Dimitri Mendeléiev, había confeccionado su tabla periódica de los elementos. Las moléculas eran demasiado pequeñas, y los químicos se veían obligados a deducir sus estructuras. Las fórmulas químicas se podían desentrañar por métodos analíticos, pero el descubrimiento de sus formas tridimensionales tuvo que esperar a la invención de la cristalografía de rayos X, una técnica que aprovecha la difracción de los rayos X para revelar la estructura de los cristales.
El científico francés Antoine Lavoisier fue el primero en demostrar que cuando se queman elementos como el fósforo y el azufre, su peso aumenta. Para comprobar la hipótesis de que incorporaban algo del aire, calentó estaño y plomo en recipientes cerrados hasta que se formó una capa sobre la superficie del metal. Sabía que esta capa, que él llamaba calx (en realidad es óxido metálico), pesaba más que los metales; pero cuando pesaba el recipiente después de calentarlo, pesaba lo mismo que antes. Si el calx era más pesado, alguna otra cosa debía haber perdido peso, tal vez el aire. Cuando quitó el tapón, penetró aire en el recipiente, y al pesarlo de nuevo comprobó que ahora pesaba más.
De este modo pudo demostrar que la combustión suponía una combinación del material quemado con algún componente del aire, y que el conjunto del sistema no ganaba ni perdía masa. Había establecido la naturaleza de la combustión y la ley de la conservación de la masa. Lavoisier llegó a la conclusión de que el aire estaba formado por: oxígeno, que intervenía en la combustión, y nitrógeno, que no intervenía.

Movimiento browniano
En 1827, el botánico escocés Robert Brown examinaba unos granos de polen al microscopio cuando se dio cuenta de que se movían al azar en la preparación. Al principio pensó que estaban vivos, pero luego repitió el experimento con granos de colorante, con el mismo resultado. Brown no encontró explicación, pero después de 1860 el físico escocés James Clerk Maxwell, halló una. Según la teoría molecular de los gases, formulada por Maxwell, eran los movimientos de las moléculas de agua los que hacían que se movieran los granos de polen. En 1905 Albert Einstein elaboró la teoría matemáticamente, y tres años más tarde, el químico francés Jean Perrin la utilizó para calcular el tamaño de las moléculas; fue la primera prueba física de las moléculas.
Pesos atómicos
El primer estudio sistemático del peso de los átomos lo llevó a cabo Johan Jakob Berzelius, que publicó tablas de pesos atómicos en 1814, 1818 y 1826. Utilizó como criterio de comparación el oxígeno, por la cantidad de compuestos que lo contenían, y le asignó el valor de 100. Aislando los elementos de un compuesto y pesándolos, él deducía la fórmula del compuesto y pudo calcular muchos pesos atómicos con un grado razonable de exactitud.

En 1811, el químico italiano Amedeo Avogadro propuso la hipótesis de que un determinado volumen de gas contenía el mismo número de partículas. Puede que no fueran átomos individuales, pero podrían ser combinaciones de átomos, es decir, moléculas. Esta teoría, defendida en el Congreso de Química de Karlsruhe de 1860 por el también italiano Stanislao Cannizzaro, proporcionó un método muy útil para calcular pesos atómicos.
La medición química de los pesos atómicos alcanzó su culminación con los trabajos del químico norteamericano Theodore Richards, que, con su equipo de colaboradores, se pasó casi 30 años determinando los pesos atómicos de 60 elementos, con una precisión sin precedentes.
Vitalismo
La idea de que los seres vivos difieren fundamentalmente de los inanimados, siguen leyes científicas diferentes y están animados por una «fuerza vital», es una herejía científica con un largo historial. Uno de sus primeros defensores fue el químico alemán Georg Stahl. El vitalismo estuvo muy en boga en los primeros años del siglo XIX. Numerosos químicos argumentaban que los compuestos orgánicos característicos de la vida no se pueden producir sin una fuerza vital que existe en las plantas y los animales.

Los vitalistas alegaban que la fermentación era imposible sin la presencia de levaduras vivas. Pero otro químico alemán, Eduard Büchner, lo desmintió en 1896, triturando levaduras hasta tal punto que no quedaran células vivas y demostrando que aún eran capaces de provocar la fermentación. Los “fermentos” de Büchner (ahora llamados enzimas) eran sustancias químicas que no poseían ninguna fuerza vital. Sin embargo, a pesar de estas demostraciones, el vitalismo no ha muerto; mucha gente prefiere creer que los seres vivos son algo más que máquinas químicas.
La tabla periódica
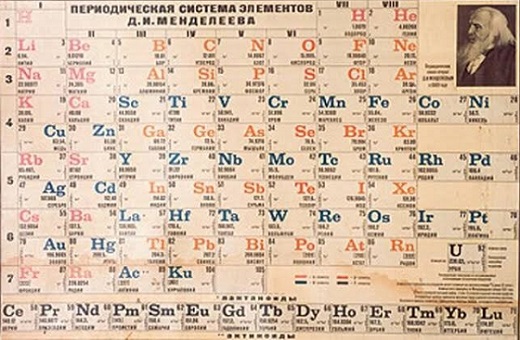
Al ir aumentando el número de elementos conocidos, los químicos buscaron maneras de organizarlos de un modo sistemático, que reflejara sus pesos atómicos y sus propiedades. El geólogo francés Béguyer de Chancourtois y el químico inglés John Newlands, elaboraron sendas tablas, en las que ordenaron los elementos por su peso atómico. Pero el mérito de la clasificación correcta de los elementos le corresponde por derecho al ruso Dimitri Mendeléiev.
Aunque no presentó su tabla hasta 1869 (y una versión corregida en 1871), Mendeléiev estaba tan seguro de su validez que no vaciló en dejar huecos donde pensaba que debían situarse elementos aún no descubiertos, ni en colocar elementos fuera del orden estricto si sus propiedades así lo recomendaban. Dejó tres huecos, anunciando las propiedades de los elementos que algún día los ocuparían. Y tal como él predijo, se descubrieron el galio en 1875, el escandio en 1879 y el germanio en 1886. Su fama estaba asegurada. En su tabla periódica, Dimitri Mendeléiev ordenó los elementos en hileras de peso atómico creciente y columnas de propiedades similares.
El malva de Perkin y la química sintética
En 1856, a los 18 años de edad, el químico inglés William Perkin, descubrió el primer colorante sintético, y este acontecimiento señaló el nacimiento de la industria química. Perkin trabajaba con el científico alemán August Hofmann en la Facultad de Química de Londres. Hofmann se había preguntado en voz alta si sería posible sintetizar quinina a partir de alquitrán de carbón, un subproducto de la industria del gas de carbón. El día de Pascua de 1856, en un laboratorio que había montado en su casa, Perkin intentó sintetizar quinina mediante la oxidación de anilina, y obtuvo un precipitado negro. Cuando estaba a punto de tirarlo, observó un destello violáceo. Añadió alcohol y obtuvo un hermoso colorante violeta.
Se lo envió a John Pullar and Son, de Perth, una empresa tintorera escocesa. En su carta de respuesta, Robert Pullar decía: “Si su descubrimiento no encarece demasiado los artículos, es sin duda uno de los más valiosos que han surgido en bastante tiempo”. Perkin abandonó la facultad, fundó una fábrica y en 1857 empezó a producir su colorante. Al principio, los clientes ingleses se mostraron escépticos, pero los tintoreros franceses se entusiasmaron, y llamaron al color «malva» y a la sustancia química «malvina». A los 35 años, Perkin se había enriquecido lo suficiente para vender la empresa y dedicarse por entero a la química.

Radiactividad e isótopos
En 1896 el físico francés Antoine Henri Becquerel, descubrió por casualidad que las sales de uranio emiten una fuerte radiación. Había descubierto la radiactividad. Poco después, el químico inglés William Crookes descubrió que el uranio purificado se descompone en dos sustancias, una de ellas mucho más radiactiva que la otra. A continuación, Becquerel demostró que, si se deja en reposo durante algún tiempo la forma menos radiactiva, su radiactividad aumenta. El neozelandés Ernest Rutherford y el químico inglés Frederick Soddy, sugirieron que los elementos radiactivos se van transformando a medida que emiten radiactividad.
Algunos de los elementos transformados parecían químicamente idénticos a elementos existentes. En 1913 Soddy proclamó que los elementos pueden existir en más de una forma, químicamente idénticas, pero con distinta masa; a estas formas alternativas las llamó: isótopos.

Cristalografía de rayos X
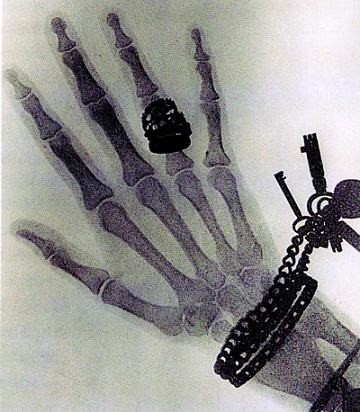
En 1895 el físico alemán Wilhelm Röntgen, descubrió los rayos X al comprobar que un tubo de rayos catódicos emitía una radiación desconocida, capaz de provocar un resplandor en los objetos luminiscentes, incluso a través de un cartón. En siete semanas de frenética actividad, desentrañó las propiedades fundamentales de los rayos, pero, no sabiendo lo que eran, los llamó X. El descubrimiento proporcionó la primera posibilidad de observar el esqueleto a través de los tejidos blandos. El 23 de enero de 1896 en Würzburg, Alemania, Röntgen pronuncia una conferencia ante la Sociedad de Física y Medicina para la divulgar el descubrimiento de los rayos X.
Químicos y físicos se dedicaron de inmediato a estudiar los rayos X, investigando si se comportaban como la luz. Uno de los métodos consistía en observar si se podían difractar (desviar) haciéndolos pasar por una rejilla de espacios muy pequeños. Esto sólo funciona si el espaciado de la rejilla es aproximadamente igual a la longitud de onda de la radiación, y el poder de penetración de los rayos X parecía indicar que su longitud de onda era corta.
El físico alemán Max von Laue, pensó que los cristales, con sus átomos uniformemente espaciados, podrían servir para difractar los rayos X. En 1912 lo intentó con un cristal de sulfuro de cinc y comprobó que funcionaba. En 1915 el científico inglés William Bragg y su hijo Lawrence, utilizaron la difracción de los rayos X para desentrañar la estructura de cristales desconocidos, inventando la potente técnica de la cristalografía de rayos X. Los rayos X sirvieron para aclarar confusiones en la tabla periódica. En 1914 el físico inglés Henry Moseley, aprovechó el hecho de que los diferentes elementos emiten rayos X de diferentes longitudes de onda para ordenar definitivamente los elementos, dejando espacios en los lugares adecuados.
Plásticos y fibras artificiales
La era del plástico comenzó en 1862, cuando el químico británico Alexander Parkes, sintetizó nitrato de celulosa, tratando celulosa (material de la madera) con ácido nítrico. Con la adición de alcanfor y bajo el nombre de celuloide, el nuevo producto se utilizó para fabricar juguetes, cuellos y puños de camisa y pelotas de ping-pong.
El primer plástico totalmente sintético fue la baquelita, sintetizada en 1905 por el químico de origen belga Leo Hendrik Baekeland, mezclando fenol y formaldehído. La baquelita era un material resinoso que se podía moldear a base de calor y presión, y se utilizó para fabricar teléfonos. En 1930 varios químicos ingleses, canadienses y alemanes descubrieron que el metacrilato se podía polimerizar para producir un plástico transparente, el perspex. En Gran Bretaña descubrieron en 1935 el polietileno, y aquel mismo año, el estadounidense Wallace Carothers, sintetizó el nailon, haciendo reaccionar ácido adípico con Hexametilendiamida.


Últimos Articulos
- Mapa de Colombia: Áreas protegidas
- Mapa de Brasil: Regiones administrativas
- Mapa Brasil: Regiones naturales
- Mapa de Argentina: Regiones naturales
- Mapa ecológico de Colombia
- Mapa cultural de Colombia para colorear
- Mapa de Colombia: Topografía
- Mapa de Chile Tricontinental
- Mapa de Bolivia: Regiones naturales
- Mapa de Chile: Regiones naturales
- Mapa de Paraguay: Regiones naturales
- Mapa de Ecuador: Regiones naturales
- Mapa de Venezuela: Regiones naturales
- Roma monárquica: Otros pueblos itálicos
- Roma monárquica: Los etruscos
Notas de interés
- Mapa de Colombia: Áreas protegidas
- Mapa de Brasil: Regiones administrativas
- Mapa Brasil: Regiones naturales
- Mapa de Argentina: Regiones naturales
- Mapa ecológico de Colombia
- Mapa cultural de Colombia para colorear
- Mapa de Colombia: Topografía
- Mapa de Chile Tricontinental
- Mapa de Bolivia: Regiones naturales
- Mapa de Chile: Regiones naturales
- Mapa de Paraguay: Regiones naturales
- Mapa de Ecuador: Regiones naturales
- Mapa de Venezuela: Regiones naturales
- Roma monárquica: Otros pueblos itálicos
- Roma monárquica: Los etruscos
- Roma monárquica: La Reforma de Servio Tulio
- Roma monárquica: La guerra contra los sabinos
- Roma monárquica: Los siete reyes
- Mapa de Colombia: Departamentos, capitales y ciudades importantes
- Mapa de Perú: Regiones naturales
Historia
- Religiones: Budismo
- La sociología
- Romanticismo y subjetivismo
- Historia del pesebre de navidad
- Día internacional de la mujer
- Historia de la filosofía: Renacimiento e Ilustración
- Historia de la física moderna
- Religiones: Cristianismo I
- Historia del Halloween
- La psicología
- Historia de la química moderna
- Idealismo contra materialismo
- Historia de la filosofía: Siglos XIX y XX
- Religiones: Cristianismo III. Protestantismos
- El estudio de la historia
- Historia de la medicina moderna
- Religiones: Cristianismo IV. Iglesias ortodoxas
- Religiones: Hinduismo
- Religiones: Shintoísmo
- Religiones: Taoísmo
- Religiones: Cristianismo II. La iglesia católica
- ¿Qué es la historia?
- Antropología cultural
- Antropología física
- El estudio de la evolución
- Historia de la filosofía: Grecia y Roma
- Historia de la filosofía: La escolástica medieval
- La historia y el oficio del historiador
- La religión
- Religiones: Confucianismo
- Religiones: Judaísmo




